- 集团首页
- 公司首页
-
关于我们
- 团队队伍
- 科学研究
- 旗下产业
- 研究生教育
- 党群工作
当前位置: 首页 >>
冯莹柱, 男, 中共党员, 工学博士, 副教授(药学), 实验室负责人。重庆市英才计划, 优秀留学回国人员, 重庆大学员工联盟会会员。2005年6月考入重庆大学(CQU)生物工程公司硕博连读; 2009年11月~2012年3月博士在读期间赴美国约翰霍普金斯大学医公司药理分子科学系高通量筛选中心(Johns Hopkins University, Medical School, HIT Center)进行博士联合培养, 主要采用膜蛋白融合策略(membrane protein fusion strategy), Red/ET, DNA重组基因编辑技术, 高通量gate-way克隆技术, 构建人膜蛋白重组病毒芯片(VirD-GPCRs, G蛋白偶联受体微阵列>800), 并提出拓展构建VirD-cytokines (人细胞因子病毒微阵列>300), VirD-enzymes (人蛋白酶病毒微阵列>800) 和 VirD-polymers (蛋白聚合物病毒微阵列) 应用到化合物(molecular drugs), 抗体(antibody), 分子配体(ligand), 凝集素(lectin) 超高通量, 大规模的药物活性筛选 (Anal. Chem. 2024); 构建细菌E.coli芯片; 细胞化学因子&芯片&电化学振荡器; 人类蛋白质组重组病毒芯片(VirD-HuprotTM/Huprot>18000 prs) 开展病原菌与宿主细胞相互作用的研究, 2013年6月获得中美联合培养博士学位。博士毕业后, 先后在上海交通大学太阳成集团tyc151cc和中国科公司上海生命科学研究院生化细胞研究所从事博士后研究, 研究领域为分子识别, 肿瘤核质穿梭分子定位, 膜蛋白互作调控机制, 基因启动子代谢工程; 后在中山老员工命科学公司担任副研究员。2019年9月加入太阳成集团tyc151cc创新靶向药物国际研究院工作, 主要建立NLRP蛋白家族的免疫炎症调控的分析研究平台; 发展泛素化蛋白(Ub)激活细胞自噬的生物相变研究(分子相互作用), “动态凝聚体”, 蛋白互作调控网络, 荧光探针标记探究配体-受体的作用生物力。拟通过对这些生物过程的调控, 提取高生物活性的蛋白多肽类药物。整合计算机蛋白质药物设计的优势资源, 发展新兴交叉学科前沿研究领域, 为新冠病毒(Covid-19)疫情等感染性疾病的防控提供理论指导与借鉴, 为药物高通量高内涵筛选, 新型药物设计研发, 光电功能材料, 膜表界面修饰材料的拓展研究与应用; 蛋白外泌体,寡聚体与生物标志物分析, 重大疾病的诊断与治疗提供新的思路, 方法与技术。从事研究工作以来在国际分析化学领域Top期刊《Analytical Chemistry》发表一作&共同一作论文2篇 (中科院SCI一区, IF:8.1), 一共发表国内外重要论文20篇, 其中第一作者论文12篇。论文在Web Of Science核心合集中被引共计39频次。主持并参与各类省部级研究课题共10项。作为副主编出版国家级教材1部, 作为参与人授权发明专利2项。已完成8名制药工程本科员工毕业论文指导和3篇全国毕业论文抽检。拟承担生物化学与分子生物学, 分子生物力学, 药理学或药物分析本科或硕士教学任务。研究成果具有广泛生物医药应用的前景与价值。
一、教育背景与工作经历
1.09/2005 – 06/2013, 重庆大学(Chongqing University), 重庆 , 硕士 , 博士, 生物医学工程, 导师:王伯初教授
2. 11/2009 – 03/2012, 美国约翰霍普金斯大学( Johns Hopkins University, USA),生物医学工程, 中美联合培养博士, 导师:朱衡教授 (Prof. Heng Zhu)
3. 10/2013– 07/2015 上海交通大学 (Shanghai Jiao Tong University), 博士后, 导师:傅磊教授(中国博士后科学基金资助二等资助)
二、主持在研的课题
1. 重庆市自然科学基金, cstc2021jcyj-msxmX0438, 细胞因子RANTES(CCL−5)激活G蛋白偶联受体(GPCR75)促进胰岛素高通量分泌的生物力化学调控机制研究, 10w, 在研。
2. 重庆市教委研究计划, KJQN202001334, IbeC膜蛋白对大肠杆菌Escherichia coli(E.coli)侵入人血脑屏障的影响, 4w, 在研。
3. 重庆老员工物流变科学与技术教育部重点实验室, CQKLBST-2020-004, 构建O-linked聚糖修饰的Spike与ACE2膜蛋白的非感染性重组疱疹病毒(HSV-1, K082)应用于新冠肺炎患者双靶点抗体药物研发, 4w, 在研。
4.永川区自然科学基金, YCSTC, 2020nb0219, 灭活的新冠病毒和重组新型冠状病毒2019-nCoV Coronavirus (2019-nCoV)膜蛋白的非感染性疱疹病毒(HSV-1, K082)诱导的综合抗体诊疗方法, 2w, 在研。
5. 太阳成集团tyc151cc塔基计划-引进人才项目, R2019SXY12, 炎症抑制蛋白NLRP2与溶血磷脂蛋白受体GPCR(G2A)交互作用的新颖分子机制研究, 8w, 在研。
6.永川区技术创新与应用发展项目, 2025yc-cxfz10103, 发展一种新的高灵敏的氢氚交换和纯化亲和质谱研究蛋白质的构象和生物相变, 8w, 在研。
三、近年代表论文
1. High−Throughput Chip Assay for Investigating Escherichia coli Interaction with the Blood−Brain Barrier Using Microbial and Human Proteome Microarrays (Dual-Microarray Technology), Analytical Chemistry, 中科院一区(IF: 8.1), 2018,90(18):10958-10966, 第一作者。
2. VirD −A Virion Display Array for Profiling Functional Human Membrane Proteins, Analytical Chemistry, 中科院一区(IF: 8.1), 2013, 85(17): 8046-8054, 第一作者。
3. Future Perspective: High Throughput Construction of New Ultra Sensitive Cytokine and Virion Liquid Chips for High Throughput Screening (HTS) Anti-inflammation Drugs or Clinical Diagnosis and Therapy of Inflammatory Diseases, Analytical Bioanalytical Chemistry, 中科院二区, 2020, 28(412): 7685-7699, 第一作者&通讯作者。
4. The Applications of Promoter-gene-Engineered Biosensors, Sensors, 中科院三区, 2018, Aug 27;18(9). pii: E2823. 第一作者。
5. Pilot Study on the Chemical Inducible Promoter-Biosensor to Promote Biosynthesis of Valuable Medicinal Compound, Journal Experimental Clinical Microbiology, 2019, 2(2): 16-28, 第一作者。
6. High-throughput Approaches to Detect Cytokines and Chemokines Secretion by Both Autophagy and Endosome Vesicle Fusion of HBMEC by Knocking Down the NLRP2 Gene, Current Analytical Chemistry, 2025,21(5):478-520, 第一作者&通讯作者。
7. 微生物学实验(教材), 北京,冶金工业出版(教材/国家级出版社), ISBN:978-7-5024-8546-7, 编著病毒学/第九章, 副主编。
四、参与平台与创新团队建设, 促进公司与企业联合联动研究
高通量光电化学芯片&电化学-应用高通量蛋白质芯片分析方法研究重大疾病的分子机制
① 构建E.coli芯片与人类蛋白质组芯片 (Huprot>18000, 如膜蛋白融合策略) 研究膜蛋白互作介导的病原菌(E.coli)与宿主细胞(HBMEC)的相互作用, 为发展抗病毒/细菌, 抗肿瘤药物提供理论依据 (Figure 1)。
Title: High-Throughput Chip Assay for Investigating Escherichia coli Interaction with the Blood−Brain−Barrier Using Microbial and Human Proteome Microarrays (Dual-Microarray Technology), 第一作者 (Analytical Chemistry 中科院: 一区, IF: 8.1)
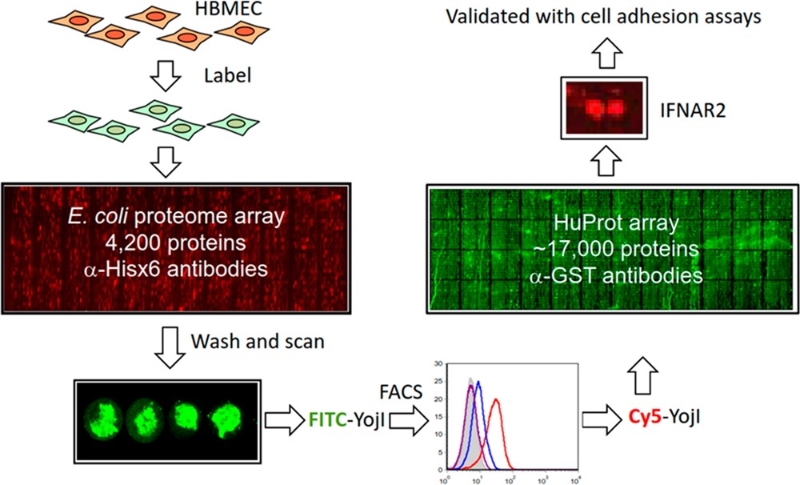
Figure 1. Utilization of E. coli and human proteome arrays to identify YojI and interferon-alpha receptor (IFNAR2) mediated bacterium host cell interactions. Live HBMEC was labeled with Vybrant CFDA SE cell tracer and probed to the E. coli proteome microarrays. As one of the E. coli membrane proteins that could capture the labeled HBMEC, YojI’s interaction with HBMEC was further validated using additional methods, such as FACS. To identify the host receptors of YojI, purified YojI proteins were fluorescently labeled and probed to the HuProt arrays, comprised of ∼18 000 human individually purified proteins. One of the identified human proteins, IFNAR2, was validated with cell adhesion assays. Each assay was performed in triplicate.
② 构建重组人类蛋白质组病毒芯片(VirD-HuprotTM)应用药物的超高通量筛选与重大疾病的诊断与治疗
构建人膜蛋白重组病毒芯片GPCR-virion chip (人膜蛋白GPCR>800), VirD-cytokines (人细胞因子>300) and VirD-enzymes (人蛋白酶>800)应用药物, 抗体(antibody), 分子配体(ligand), 凝集素(lectin)的高通量, 大规模筛选 (High Throughput Screening, HTS), 快速发现新的先导化合物与药物作用靶标; 重组人膜蛋白病毒GPCRs (>800) 可应用抗体与疫苗多肽药物的研发, 应用到各种疾病的临床诊疗(Figure 2)。
Title: VirD: A Virion Display Array for Profiling Functional Membrane Proteins, 共同第一作者 (Analytical Chemistry, 中科院: 一区, IF: 8.1)
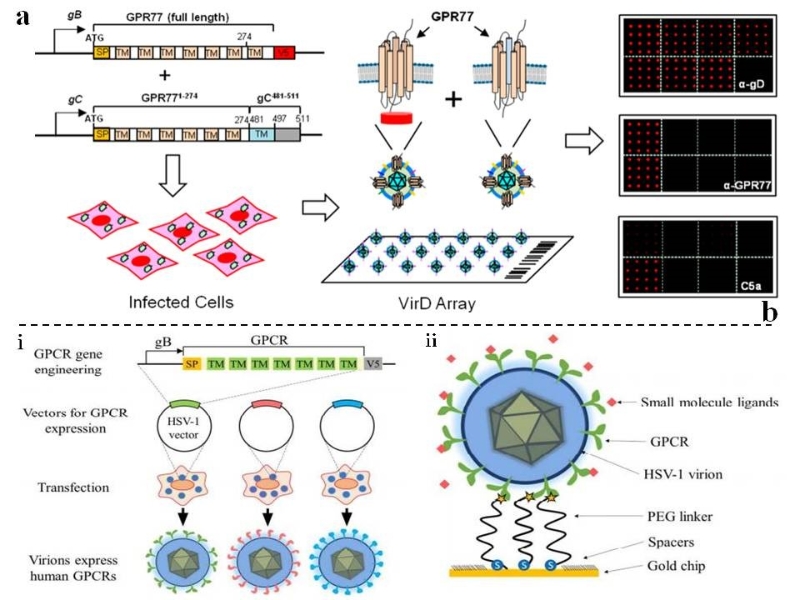
Figure 2. a. Development of the VirD Array. Schematics of the two strategies used for the virion display system are shown. The first utilizes expression of the CDs/GPR77 molecules tagged with the V5 epitope from the gB promoter, and the second uses a chimeric expression method by fusing the CDs /GPR77 to the TM and C-terminus of glycoprotein C. The signal peptide (SP) is shown. Recombinant HSV-1 virions expressing these engineered human genes were used to infect mammalian cells, and virions released from these cells, which would incorporate the human membrane protein in the virion envelope, were purified and printed on FAST slides (AC). b. Integration of virion display (VirD) with virion-oscillators for studying membrane proteins and HTS drugs. (i) Displaying human GPCRs on HSV-1 envelope with VirD. (ii) Fabricating virion-oscillators. Each virion-oscillator consisting of a virion tethered to a gold surface with 63 nm long polyethylene glycol (PEG) linkers. The PEG linker contains a thiol and a N-hydroxysuccinimide (NHS) on its two ends, where the thiol group binds to the gold surface, and the NHS group crosslinks the virion via NHS-amine reaction (JACS).
③ NLRP2 炎症分子机制与生物相变研究 (泛素化与自噬的调控)
主要围绕 NLRP2蛋白开展炎症分子机制, 免疫细胞调控, 生物相变与泛素化研究(分子相互作用力), 探究受体-配体的作用生物力, 泛素化与自噬机制的关联机制。拟通过对这些生物过程的调控, 提取有高生物医药活性的蛋白多肽类药物。经初步研究发现该蛋白是一个免疫调控的相变蛋白, 并迁移到微生物, 动植物蛋白质修饰领域的研究 (Figure 3)。为了研究 NLRP2 基因的免疫调控机制, NLRP2蛋白的自组装过程, 分别构建了NLRP2:shRNA和 NLRP2: eGFP 慢病毒感染人脑微血管内皮细胞, 负对照组和阳性对照分别用INF39与LPS药物处理后, 采用激光共聚焦(ZEISS-ISM900)和生物透射电子显微镜(TEM)观察, 可以显微观察到病毒结构, 细胞凋亡小体, 细胞内囊泡, 外泌体, 微管, 炎症蛋白等分子结构, 为探究泛素化蛋白激活细胞自噬的生物相变的分子机理提供可靠的理论依据。采用基质辅助激光解吸-飞行时间质谱仪(MALDI-TOF), HPLC-MS分析检测核酸, 蛋白质, 多肽序列, 高通量的提取获得细胞因子, 开发调控细胞自噬和生物相变的化学药物 (Figure 3,4,5)。
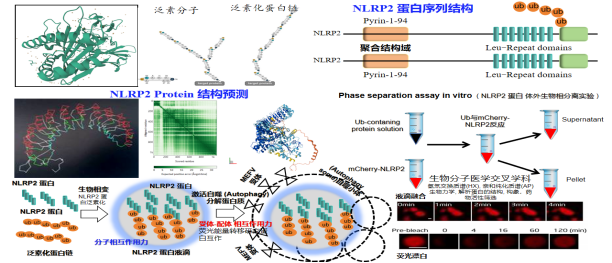
Figure 3. NLRP2protein structure prediction and poly-ubiquitin chain-induced phase separation and autophagy to promote secretion of cytokines, e.g. IL-1β/IL-18/RANTES
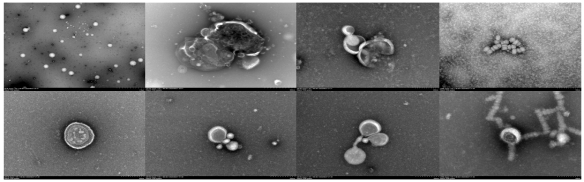
Figure 4. Cryo-electron microscopy structures from human brain microvascular endothelial cells(HBMEC) infected by the NLRP2:shRNA and NLRP2: eGFP lentivirus
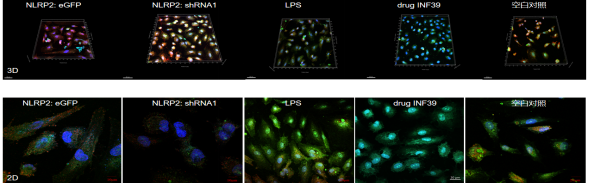
Figure 5. Co-focal microscrope map of lentivirus infecting HBMEC and drug INF39 and LPS treated
为了发展新兴生物医药研究领域, 积极推动科技创新与学科交叉融合, 教研产联动相长。发展一流学科, 发展关联人民生命健康与国家重大需求的急需的生物医药紧缺领域 (e.g重组人类蛋白病毒芯片, 蛋白质组芯片, 高通量, 高内涵药物筛选与新药研发, 生物相变与化药干预与重大疾病诊疗, 细胞因子多肽药物与新冠病毒Covid-19疫情防控), 促进"百队博士进百企"行动计划增质增效, 促进重庆市医药经济产业的快速发展与更新升级。
- 团队队伍